奏鸣曲:治疗失眠(完整的处方信息)
品牌名称:索纳塔
通用名称:Zaleplon
内容:
描述
临床药理学
适应症和用法
禁忌症
警告
预防措施
不良反应
药物滥用和依赖
过剂量
用量和给药
如何提供
索纳塔患者信息表(说白了)
描述
Zaleplon是一种非苯二氮平类催眠药,属于吡唑嘧啶类。扎来普隆的化学名称是N-[3-(3-氰吡唑啉[1,5-a]嘧啶-7-基)苯基]-N-乙基乙酰胺。它的经验公式是C17H15N5O,分子量为305.34。结构公式如下所示。
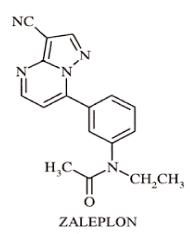
Zaleplon是一种白色或灰白色粉末,几乎不溶于水,少量溶于酒精或丙二醇。在1 ~ 7的pH范围内,它在辛醇/水中的分配系数为常数(log PC = 1.23)。
奏鸣曲®胶囊含有扎来普隆作为有效成分。非活性成分包括微晶纤维素、预糊化淀粉、二氧化硅、十二烷基硫酸钠、硬脂酸镁、乳糖、明胶、二氧化钛、D&C黄#10、FD&C蓝#1、FD&C绿#3和FD&C黄#5。
临床药理学
药效学及作用机制
虽然索纳塔(zaleplon)是一种催眠剂,其化学结构与苯二氮卓类药物、巴比妥酸盐或其他已知催眠性质的药物无关,但它与γ -氨基丁酸-苯二氮卓(GABA-BZ)受体复合物相互作用。GABA-BZ受体氯通道大分子复合物的亚单位调节被假设是苯二氮卓类药物的一些药理特性的原因,包括镇静、抗焦虑、肌肉松弛和抗惊厥作用的动物模型。
其他非临床研究也表明,zaleplon选择性地结合到位于GABAA/氯离子通道受体复合物的α亚基上的大脑-1受体,并增强t-丁基-双环硫代酸(TBPS)的结合。扎来普隆与重组GABAA受体(α1β1γ2 [ω -1]和α2β1γ2 [ω -2])结合的研究表明,扎来普隆对这些受体具有低亲和力,优先与ω -1受体结合。
药物动力学
已在500多名健康受试者(年轻人和老年人)、哺乳母亲和肝病或肾病患者中研究了扎来普隆的药代动力学。在健康受试者中,在单次给药高达60mg后,每天一次以15mg和30mg给药10天,检查了药代动力学特征。Zaleplon被迅速吸收,有一段时间达到峰值浓度(t马克斯)约1小时,终末相消除半衰期(t1/2),大约一小时。扎来普隆每日一次给药不会累积,其药代动力学在治疗范围内与剂量成正比。
吸收
口服后,扎来普隆几乎完全被迅速吸收。口服给药后约1小时内达到血药浓度峰值。虽然扎来普隆吸收良好,但其绝对生物利用度约为30%,因为它经历了显著的系统前代谢。
分布
Zaleplon是一种亲脂性化合物,静脉给药后体积分布约为1.4 L/kg,表明大量分布于血管外组织。体外血浆蛋白结合约为60%±15%,在10 ng/mL至1000 ng/mL范围内与zaleplon浓度无关。这表明扎来普隆的性格对蛋白质结合的改变不敏感。扎来普隆的血浆比约为1,表明扎来普隆均匀分布在整个血液中,没有广泛分布到红细胞中。
新陈代谢
口服后,扎来普隆被广泛代谢,只有不到1%的剂量通过尿液排出体外。扎来普隆主要由醛氧化酶代谢生成5-oxo-扎来普隆。扎来普隆在较小程度上被细胞色素P450 (CYP) 3A4代谢形成去乙基扎来普隆,该物质可能通过醛氧化酶迅速转化为5-氧基去乙基扎来普隆。这些氧化代谢产物随后转化为葡萄糖醛酸酯并在尿液中消除。扎来普隆的所有代谢物都没有药理活性。
消除
口服或静脉给药后,扎来普隆迅速消除,平均t1/2约为1小时。扎来普隆口服血浆清除率约为3 L/h/kg,静脉注射血浆清除率约为1 L/h/kg。假设肝血流量正常,扎来普隆的肾清除率可忽略,估计扎来普隆的肝抽提比约为0.7,表明扎来普隆具有较高的首通代谢。
在给予放射标记剂量的扎来普隆后,70%的给药剂量在48小时内从尿液中恢复(71%在6天内恢复),几乎全部为扎来普隆代谢物及其葡萄糖醛酸酯。另外17%在6天内从粪便中回收,大多数为5-oxo-zaleplon。
食物的作用
在健康成人中,高脂肪/高脂肪膳食与禁食状态相比,延长了扎来普隆的吸收,延迟了t马克斯缩短约2小时,减少C马克斯大约35%。Zaleplon AUC和消除半衰期无显著影响。这些结果表明,如果与高脂肪/高脂肪膳食一起服用或在进食后立即服用,索纳塔对睡眠的影响可能会降低。
特殊人群
年龄:Sonata (zaleplon)的药代动力学在三个年龄在65 - 85岁的老年男性和女性中进行了研究。索纳塔在老年受试者(包括75岁以上的老年人)中的药代动力学与年轻健康受试者的药代动力学无显著差异。
性别:索纳塔在男性和女性的药代动力学无显著差异。
种族:扎来普隆的药代动力学已在日本受试者中作为亚洲人群的代表进行了研究。对于这个基团,C马克斯AUC分别增加37%和64%。这一发现可能是由于体重的差异,或者也可能是由于饮食、环境或其他因素的差异导致的酶活性的差异。种族对其他种族群体药代动力学特征的影响尚未得到很好的表征。
肝损害:扎来普隆主要由肝脏代谢,并经历显著的系统前代谢。结果,在肝硬化代偿期和失代偿期患者中,扎来普隆的口服清除率分别降低了70%和87%,导致平均C值显著升高马克斯AUC(代偿和失代偿患者分别高达4倍和7倍),与健康受试者相比。因此,轻度至中度肝损害患者应减少索纳塔的剂量用量和给药).严重肝功能损害患者不建议使用索纳塔。
肾损害:由于未改变的扎来普隆肾排泄量占给药剂量的1%以下,因此在肾功能不全患者中,扎来普隆的药代动力学没有改变。轻中度肾损害患者不需要调整剂量。Sonata在严重肾损害患者中的研究还不够充分。
药物之间相互作用
因为扎来普隆主要由醛氧化酶代谢,在较小程度上由CYP3A4代谢,这些酶的抑制剂可能会降低扎来普隆的清除率,而这些酶的诱导剂可能会增加其清除率。扎来普隆已被证明对华法林(R型和S型)、丙咪嗪、乙醇、布洛芬、苯海拉明、硫硝嗪和地高辛的动力学影响最小。然而,扎来普隆对其他药物代谢相关酶的抑制作用尚未被研究。(见下面的药物相互作用预防措施.)
临床试验
支持有效性的对照试验
在12项安慰剂和活性药物对照试验中,Sonata(通常以5 mg、10 mg或20 mg的剂量给药)已在慢性失眠症患者(n = 3435)中进行了研究。其中三项试验是在老年患者中进行的(n = 1019)。在短暂性失眠症中也有研究(n = 264)。由于其半衰期非常短,研究集中在减少睡眠潜伏期,较少关注睡眠持续时间和唤醒次数,这与安慰剂没有一致的差异。还进行了研究,以检查对记忆和精神运动功能的影响的时间过程,并检查戒断现象。
瞬态失眠
在睡眠实验室的第一晚出现短暂性失眠的正常成年人在双盲平行组试验中进行了评估,比较了两种剂量的索纳塔(5毫克和10毫克)与安慰剂的效果。索纳塔10毫克,而不是5毫克,在降低持续睡眠潜伏期(LPS)方面优于安慰剂,这是一种多导睡眠描记术测量睡眠开始时间的方法。
慢性失眠
费用的患者:
慢性失眠的成年门诊患者在三个双盲平行组门诊研究中进行了评估,一个为期2周,两个为期4周,比较了5 mg剂量的Sonata(在两项研究中),10 mg和20 mg剂量的安慰剂对睡眠开始时间(TSO)的主观测量的影响。索纳塔10mg和20mg在TSO方面始终优于安慰剂,通常在所有三项研究的整个期间都是如此。虽然两种剂量都有效,但20毫克剂量的效果更大,更一致。5mg剂量的效果不如10mg和20mg剂量的效果一致。在这些研究中,服用索纳塔10毫克和20毫克的睡眠潜伏期比服用安慰剂的睡眠潜伏期短10-20分钟(15%-30%)。
成人门诊慢性失眠症患者在六项双盲、平行组睡眠实验室研究中进行了评估,研究持续时间从单晚到35晚不等。总的来说,这些研究表明,在治疗的前2晚,索纳塔10mg和20mg在减少LPS方面优于安慰剂。在5晚、14晚和28晚的研究中,观察到所有治疗组(包括安慰剂组)的LPS较基线水平下降,因此,Sonata与安慰剂之间的显著差异没有超过2晚。在一项35晚的研究中,在第29和30晚的主要疗效终点上,索纳塔10 mg在减少LPS方面明显比安慰剂更有效。
老年患者:
在两项为期2周的双盲平行组门诊研究中,对患有慢性失眠的老年门诊患者进行了评估,比较了索纳塔5mg和10mg与安慰剂对入睡时间(TSO)的主观测量的影响。两种剂量的索纳塔在TSO上都优于安慰剂,通常在两项研究的整个过程中都是如此,其效应大小通常与在年轻人中观察到的效应大小相似。10mg剂量在降低TSO方面有更大的效果。
慢性失眠的门诊老年患者也在2晚睡眠实验室研究中进行了评估,剂量为5mg和10mg。5毫克和10毫克剂量的索纳塔在减少持续睡眠潜伏期(LPS)方面优于安慰剂。
一般来说,在这些研究中,与基线相比,所有治疗组(包括安慰剂组)的睡眠时间都略有增加,因此,没有证明与安慰剂组在睡眠时间上有显著差异。
有关镇静/催眠药物安全问题的研究
记忆障碍
研究涉及正常受试者暴露于单一固定剂量的索纳塔(10mg或20mg),并在给药后的固定时间(如1、2、3、4、5、8和10小时)对短期记忆进行结构化评估,通常显示在1小时内短期记忆的预期损害,这是zaleplon暴露的高峰时间,两种剂量,在20 mg后效果更大。与zaleplon的快速清除一致,在一项研究中,记忆障碍早在给药后2小时就不再存在,而在3-4小时后没有一项研究出现记忆障碍。尽管如此,在较大的上市前临床试验中自发报告的不良事件显示,Sonata和安慰剂在第二天失忆的风险上存在差异(3% vs 1%),并且该事件具有明显的剂量依赖性(见不良反应).
镇静/精神运动的影响
研究涉及正常受试者暴露于单一固定剂量的索纳塔(扎来普隆)(10毫克或20毫克),并在给药后固定时间(如1、2、3、4、5、8和10小时)对镇静和精神运动功能(如反应时间和警觉性的主观评分)进行结构化评估,通常显示预期的镇静和精神运动功能损害在1小时内,即扎来普隆暴露高峰的时间,对于这两种剂量。与扎来普隆的快速清除一致,在一项研究中,精神运动功能损害早在给药后2小时就不再存在,而在3-4小时后没有一项研究出现。在更大规模的上市前临床试验中,不良事件的自发报告并没有表明索纳塔和安慰剂在第二天嗜睡的风险方面存在差异不良反应).
戒断——焦虑和失眠
在夜间使用一段较长的时间,药效学耐受或适应催眠药的某些作用可能会发展。如果药物具有较短的消除半衰期,则可能在每晚使用之间的某个时间点出现药物或其活性代谢物的相对缺乏(即与受体部位有关)。这一系列的事件被认为是导致两项临床发现的原因,据报道,在几周的夜间使用其他快速消除的催眠药后出现:在夜间最后四分之一时间清醒增加,白天焦虑的迹象增加。
扎来普隆半衰期短,没有活性代谢物。在一项35晚睡眠实验室研究的主要疗效终点(第29和30晚),多导睡眠描记仪记录显示,在夜间最后四分之一的时间内,索纳塔组的清醒时间并不明显长于安慰剂组。在Sonata的临床试验中没有观察到白天焦虑症状的增加。在两项睡眠实验室研究中,包括14和28个夜晚剂量的索纳塔(一项研究为5毫克和10毫克,另一项研究为10毫克和20毫克)和白天焦虑的结构化评估,没有发现白天焦虑的增加。同样,在一项关于自发报告的白天焦虑的汇总分析(所有平行组,安慰剂对照研究)中,索纳塔和安慰剂之间没有观察到差异。
回弹性失眠,定义为与治疗停止后的基线相比,睡眠参数(潜伏期、总睡眠时间和唤醒次数)的剂量依赖性暂时恶化,观察短效和中效催眠药物。在停用Sonata后的第1和第2个晚上(14、28和35个晚上)和5个利用患者日记(14和28个晚上)的门诊研究中,对停用Sonata后相对于基线的反弹失眠进行了检查。总的来说,数据表明反弹性失眠可能是剂量依赖的。在20 mg时,在索纳塔治疗停止后的第一个晚上,出现了客观的(多导睡眠描记仪)和主观的(日记)反弹性失眠的证据。在停用索纳塔治疗后的第一个晚上,在5 mg和10 mg组,没有客观和极少的主观证据表明出现反弹性失眠。在所有剂量下,反弹效应似乎在停药后的第二晚消失。在35个晚上的研究中,与安慰剂组相比,10毫克和20毫克组的第一晚睡眠都有所恶化,但与基线相比没有。这种停药-突发性效应是温和的,具有慢性失眠症状复发的特征,并在停用扎来普隆后的第二晚消失。
其他退缩-涌现现象
其他戒断现象的可能性也在14至28晚的研究中进行了评估,包括睡眠实验室研究和门诊研究,以及持续6个月和12个月的开放标签研究。其中几项研究使用了苯二氮卓类药物戒断症状问卷,包括基线期和停药后的第1天和第2天。停药在操作上定义为停药后出现3种或3种以上新症状。在5 mg、10 mg或20 mg剂量下,索纳塔与安慰剂没有区别,在自发报告的戒断紧急不良事件上,索纳塔与安慰剂也没有区别。没有戒断谵妄,戒断相关的幻觉,或任何其他严重镇静/催眠戒断的表现。
适应症和用法
索纳塔适用于失眠的短期治疗。在对照临床研究中,索纳塔已被证明可将睡眠开始时间缩短至30天(见《临床试验》)临床药理学).没有证据表明它能增加总睡眠时间或减少醒来次数。
支持疗效的临床试验持续时间从一晚到5周不等。在治疗结束时,对睡眠潜伏期进行了最终的正式评估。
禁忌症
对扎来普隆或配方中的任何辅料过敏(参见预防措施).
警告
由于睡眠障碍可能是身体和/或精神障碍的表现,只有在对患者进行仔细评估后,才应开始对症治疗失眠。治疗7 - 10天后失眠仍未缓解可能表明存在原发性精神和/或医学疾病,应进行评估。失眠的恶化或新的思维或行为异常的出现可能是未被发现的精神或身体障碍的后果。这些发现是在使用镇静/催眠药物(包括索纳塔)治疗过程中出现的。由于索纳塔的一些重要不良反应似乎与剂量有关,因此使用尽可能低的有效剂量是很重要的,特别是在老年人中(见用量和给药).
据报道,使用镇静/催眠药会出现各种异常的思维和行为变化。其中一些变化可能以抑制能力下降为特征(例如,似乎与性格不符的攻击性和外向性),类似于酒精和其他中枢神经系统抑制剂产生的效果。其他报告的行为变化包括怪异行为、躁动、幻觉和人格解体。健忘症和其他神经精神症状可能会不可预测地发生。在主要抑郁症患者中,抑郁的恶化,包括自杀的想法,已被报道与镇静/催眠药的使用有关。
很少能确定上述异常行为的特定实例是药物诱导的,自发的,还是潜在的精神或身体障碍的结果。尽管如此,任何新的行为迹象或症状的出现都需要仔细和立即的评估。
在迅速减少剂量或突然停止使用镇静/催眠药后,有报道称出现了与其他中枢神经系统抑制剂药物戒断相关的体征和症状(见药物滥用和依赖).
索纳塔,像其他催眠药一样,有中枢神经抑制剂的作用。由于索纳塔起效迅速,只能在就寝前或患者入睡困难后立即服用。服用索纳塔的患者在服用该药后应避免从事需要完全精神警惕性或运动协调的危险职业(例如,操作机械或驾驶机动车),包括在服用索纳塔后的第二天可能发生的此类活动表现的潜在损害。索纳塔,以及其他催眠药,可能产生附加的中枢神经系统抑制作用时,与其他精神药物,抗惊厥药,抗组胺药,麻醉镇痛药,麻醉剂,乙醇,和其他药物本身产生中枢神经系统抑制。索纳塔不应与酒精一起服用。当索纳塔与其他cns抑制剂一起使用时,可能需要调整剂量,因为有潜在的加性作用。
预防措施
一般
给药时机
索纳塔应在就寝前立即服用,或在患者上床后难以入睡后服用。与所有镇静/催眠药一样,在起床和走动时服用索纳塔可能会导致短期记忆障碍、幻觉、协调能力受损、头晕和头晕。
适用于老年和/或虚弱的病人
在治疗老年和/或虚弱患者时,反复接触镇静/催眠药物或对镇静/催眠药物异常敏感后,运动和/或认知功能受损是一个值得关注的问题。建议老年患者服用5mg的剂量,以减少副作用的可能性用量和给药).应密切监测老年和/或虚弱患者。
用于伴有疾病的病人
在伴有全身疾病的患者中使用Sonata的临床经验有限。患有可能影响新陈代谢或血流动力学反应的疾病或病症的患者应谨慎使用索纳塔。雷竞技到底好不好用
虽然初步研究没有揭示正常受试者催眠剂量的索纳塔的呼吸抑制剂作用,但如果将索纳塔(zaleplon)开给呼吸功能受损的患者,应谨慎观察,因为镇静/催眠药有抑制呼吸驱动的能力。在轻度至中度慢性阻塞性肺疾病或中度阻塞性睡眠呼吸暂停患者中,急性给药Sonata 10mg的对照试验显示,血气或呼吸暂停/低通气指数分别没有改变的证据。然而,由于既往疾病导致呼吸功能下降的患者应仔细监测。
对于轻度至中度肝损害的患者,索纳塔的剂量应减少至5mg用量和给药).严重肝功能损害的患者不建议使用。
轻中度肾损害患者不需要调整剂量。Sonata在严重肾损害患者中的研究还不够充分。
用于抑郁症患者
与其他镇静/催眠药物一样,索纳塔对表现出抑郁症状或体征的患者应谨慎使用。这类患者可能有自杀倾向,可能需要采取保护措施。有意过量用药在这组患者中更为常见过剂量);因此,在任何时候都应该给病人开尽可能少的药。
本产品含有FD&C黄5号(酒黄石),可能会引起某些易感人群的过敏反应(包括支气管哮喘)。虽然FD&C黄5号(酒黄石)敏感性在一般人群中的总体发病率较低,但在同时具有阿司匹林过敏反应的患者中经常可见。
患者须知
病人的信息打印在这张插页的末尾。为确保安全有效地使用Sonata,应与患者讨论患者信息部分中提供的信息和说明。
实验室测试
不建议进行具体的实验室测试。
药物的相互作用
与所有药物一样,存在着通过各种机制与其他药物相互作用的潜力。
CNS-Active药物
乙醇:Sonata 10 mg增强了0.75 g/kg乙醇对乙醇给药后1小时平衡测试和反应时间的cns损害效应,以及对乙醇给药后2.5小时数字符号替换测试(DSST)、符号复制测试和分散注意测试的可变性成分的影响。增强作用源于中枢神经系统药效学的相互作用;扎来普隆不影响乙醇的药代动力学。
丙咪嗪:单剂量的索纳塔20毫克和丙咪嗪75毫克在给药后2至4小时内对警觉性下降和精神运动性能受损产生加性作用。这种相互作用是药效学上的,两种药物的药代动力学没有改变。
帕罗西汀:单剂量索纳塔20毫克和帕罗西汀20毫克,每天共给药7天,对精神运动性能没有产生任何相互作用。此外,帕罗西汀没有改变索纳塔的药代动力学,这反映了CYP2D6在扎来普隆的代谢中没有作用。
硫硝嗪:单剂量的索纳塔20 mg和硫硝嗪50 mg在给药后2 - 4小时内对警觉性下降和精神运动性能受损产生加性作用。这种相互作用是药效学上的,两种药物的药代动力学没有改变。
文拉法辛:单剂量扎来普隆10mg和多剂量文拉法辛ER(缓释)150mg的联合给药没有导致任何扎来普隆或文拉法辛的药代动力学发生显著变化。此外,由于扎来普隆和文拉法辛ER合用,没有药理学上的相互作用。
异丙嗪:单剂量扎来普隆和异丙嗪(分别为10和25 mg)共给药导致最大血浆扎来普隆浓度降低15%,但血浆浓度-时间曲线下的面积没有变化。然而,扎来普隆和异丙嗪联合给药的药效学尚未得到评估。这两种药物合用时应谨慎。
诱导CYP3A4的药物
利福平:CYP3A4通常是扎来普隆的次要代谢酶。然而,多剂量给予强效CYP3A4诱导剂利福平(每24小时600mg, q24h,持续14天)可使扎来普隆Cmax和AUC降低约80%。联合使用强效CYP3A4酶诱导剂,虽然不构成安全隐患,但可能导致扎来普隆无效。在服用利福平、苯妥英、卡马西平和苯巴比妥等CYP3A4诱导剂的患者中,可以考虑使用一种替代的非CYP3A4底物催眠药物。
抑制CYP3A4的药物
CYP3A4是消除扎来普隆的次要代谢途径,因为去乙基扎来普隆(在体外通过CYP3A4形成)及其代谢物,5-氧基去乙基扎来普隆和5-氧基去乙基扎来普隆葡萄糖醛酸盐的总量仅占扎来普隆剂量尿恢复的9%。单剂量口服zaleplon与红霉素(一种强选择性CYP3A4抑制剂)(分别为10mg和800mg)联合给药,zaleplon最大血浆浓度增加34%,血浆浓度-时间曲线下面积增加20%。与多剂量红霉素相互作用的程度尚不清楚。其他强选择性CYP3A4抑制剂如酮康唑也有望增加扎来普隆的暴露量。扎来普隆的常规剂量调整被认为是不必要的。
抑制醛氧化酶的药物
乙醛氧化酶系统的研究不如细胞色素P450酶系统。
苯海拉明:据报道苯海拉明是大鼠肝脏中醛氧化酶的弱抑制剂,但其在人肝脏中的抑制作用尚不清楚。单次给药(分别为10mg和50mg)后,扎来普隆和苯海拉明之间没有药代动力学相互作用。然而,因为这两种化合物都有中枢神经系统的影响,一种加性药效学效应是可能的。
同时抑制醛氧化酶和CYP3A4的药物
西咪替丁:西咪替丁既能抑制醛氧化酶(体外),又能抑制CYP3A4(体内外),分别是负责扎来普隆代谢的一级酶和二级酶。同时服用索纳塔(10 mg)和西咪替丁(800 mg)可使zaleplon的平均Cmax和AUC增加85%。同时使用西咪替丁治疗的患者应给予5mg的初始剂量(见用量和给药).
与血浆蛋白高度结合的药物
扎来普隆与血浆蛋白结合度不高(分数结合率为60%±15%);因此,扎来普隆的处置预计不会对蛋白质结合的改变敏感。此外,给正在服用另一种高蛋白结合药物的患者使用Sonata不应引起另一种药物游离浓度的短暂增加。
治疗指数较窄的药物
地高辛:索纳塔(10mg)不影响地高辛的药代动力学或药效学特征(0.375 mg q24h, 8天)。
华法林:多次口服剂量的索纳塔(20mg q24h,持续13天)不影响华法林(R+)-或(S-)-对映体的药代动力学或单次口服剂量25mg华法林后的药动力学(凝血酶原时间)。
改变肾脏排泄的药物
布洛芬:已知布洛芬会影响肾功能,从而改变其他药物的肾脏排泄。每种药物单次给药(分别为10mg和600mg)后,扎来普隆和布洛芬之间没有明显的药代动力学相互作用。这是意料之中的,因为扎来普隆主要是代谢的,不变的扎来普隆肾脏排泄占给药剂量的1%不到。
癌变、突变和生育力损害
致癌作用
在小鼠和大鼠中进行了扎来普隆的终生致癌性研究。小鼠分别接受25 mg/kg/天、50 mg/kg/天、100 mg/kg/天和200 mg/kg/天的饮食剂量,持续两年。这些剂量相当于人体最大推荐剂量(MRHD) 20毫克(以毫克/平方米为单位)的6至49倍。高剂量组雌性小鼠肝细胞腺瘤发生率显著增加。大鼠在饮食中分别给予1 mg/kg/天、10 mg/kg/天和20 mg/kg/天剂量,持续两年。这些剂量相当于人体最大推荐剂量(MRHD) 20毫克(以毫克/平方米为单位)的0.5至10倍。扎来普隆对大鼠没有致癌性。
诱变
在体外中国仓鼠卵巢细胞实验中检测染色体畸变时,Zaleplon在存在或不存在代谢激活的情况下都具有致裂性,导致结构和数量畸变(多倍体和核内重复)。在体外人淋巴细胞实验中,扎来普隆只在最高浓度的代谢激活下引起数值畸变,而不是结构畸变。在其他体外试验中,扎来普隆在Ames细菌基因突变试验或中国仓鼠卵巢HGPRT基因突变试验中没有致突变性。在小鼠骨髓微核试验和大鼠骨髓染色体畸变试验两项体内试验中,扎来普隆没有致裂作用,在大鼠肝细胞非定时DNA合成试验中也没有引起DNA损伤。
生育能力受损
在一项大鼠生育能力和生殖性能研究中,雄性和雌性在交配前和交配期间口服100 mg/kg/天的扎来普隆与死亡率和生育能力下降有关。这一剂量相当于人体最大推荐剂量(MRHD) 20毫克/米的49倍2的基础上。后续研究表明,生育能力受损是由于对女性的影响。
妊娠:C类妊娠
在大鼠和兔子的胚胎胚胎发育研究中,在整个器官发生过程中,对怀孕动物分别口服高达100 mg/kg/天和50 mg/kg/天,没有产生致畸性的证据。这些剂量相当于人类最大推荐剂量(MRHD)的49倍(大鼠)和48倍(兔子),以毫克/平方米为单位计算。在大鼠中,接受100 mg/kg/天剂量的母鼠后代的产前和产后生长均有所下降。这一剂量对母体也是有毒的,临床症状和妊娠期间母体体重增加减少都证明了这一点。减少大鼠后代生长的无效剂量为10 mg/kg(剂量相当于MRHD 20 mg/m的5倍2基础)。在实验剂量下,未观察到对兔胚胎发育的不良影响。
在一项大鼠产前和产后发育研究中,观察到在妊娠后期和整个哺乳期使用7 mg/kg/天或更大剂量的雌性小鼠的后代中,死胎和产后死亡率增加,生长和身体发育下降。在这个剂量下,没有证据表明产妇中毒。对后代发育无影响的剂量为1 mg/kg/天(剂量相当于MRHD 20 mg/m2的0.5倍)。当在一项交叉培养研究中检查对后代生存能力和生长的不利影响时,它们似乎是由子宫内和哺乳期暴露于药物造成的。
目前还没有关于扎来普隆对孕妇的研究;因此,奏鸣曲®(扎来普隆)不建议在怀孕期间使用。
劳动与交付
索纳塔在生产和生产中没有确定的用途。
哺乳期妇女
一项对哺乳期母亲的研究表明,扎来普隆的清除率和半衰期与年轻正常受试者相似。少量的扎来普隆在母乳中排泄,排泄量最高的发生在喂奶期间,大约在索纳塔给药后1小时。由于从母乳中提取的少量药物可能会导致婴儿体内潜在的重要浓度,而且由于扎来普隆对哺乳婴儿的影响尚不清楚,因此建议哺乳母亲不要服用索纳塔。
儿童使用
Sonata在儿科患者中的安全性和有效性尚未得到证实。
老年使用
在接受Sonata治疗的双盲、安慰剂对照、平行组临床试验中,共有628例患者年龄至少为65岁;其中311人摄入5毫克,317人摄入10毫克。在睡眠实验室和门诊研究中,老年失眠症患者对5mg剂量有反应,睡眠潜伏期降低,因此5mg是该人群的推荐剂量。在使用Sonata的老年患者的短期治疗(14个夜间研究)中,5 mg或10 mg Sonata的不良事件发生率明显高于安慰剂,发生率至少为1%。
不良反应
Sonata上市前开发项目包括来自2组不同研究的患者和/或正常受试者的扎来普隆暴露:临床药理学/药代动力学研究的约900名正常受试者;在安慰剂对照的临床疗效研究中,大约有2900名患者暴露于此,相当于大约450名患者暴露于此。Sona雷竞技到底好不好用ta治疗的条件和持续时间差异很大,包括(在重叠的类别中)开放标签和双盲研究阶段,住院患者和门诊患者,以及短期或长期暴露。通过收集不良事件、体检结果、生命体征、体重、实验室分析和心电图评估不良反应。
暴露期间的不良事件主要通过普通询问获得,并由临床研究者使用自己选择的术语进行记录。因此,如果不首先将相似类型的事件分组为数量较少的标准化事件类别,就不可能对经历不良事件的个体比例提供有意义的估计。在下面的表格中,COSTART术语已被用于对报告的不良事件进行分类。
所述不良事件的频率表示至少经历过一次所列类型的治疗突发不良事件的个体比例。如果事件是第一次发生或在基线评估后接受治疗时恶化,则认为是治疗紧急事件。
在短期安慰剂对照试验中观察到的不良结果
与停止治疗相关的不良事件
在上市前安慰剂对照、平行组2期和3期临床试验中,744名接受安慰剂的患者中有3.1%,2149名接受Sonata的患者中有3.7%,因为不良临床事件而停止治疗。这种差异没有统计学意义。没有导致终止的事件发生在≥1%。
在接受索纳塔20毫克治疗的患者中,不良事件发生率为1%或更高
表1列举了3个28夜和1个35夜的Sonata安慰剂对照研究(剂量分别为5mg或10mg和20mg)的治疗突发不良事件发生率。该表仅包括那些在接受索纳塔20mg治疗的患者中发生的1%或更多的事件,并且索纳塔20mg治疗的患者发生率高于安慰剂治疗的患者。
开处方者应意识到,这些数字不能用于预测在常规医疗实践过程中不良事件的发生率,因为患者的特征和其他因素与临床试验中普遍存在的情况不同。同样,所引用的频率不能与其他涉及不同治疗方法、用途和研究者的临床调查所得的数字进行比较。然而,所引用的数据确实为开药医生估计药物和非药物因素对研究人群不良事件发生率的相对贡献提供了一些依据。
| 身体系统 | 安慰剂 | 索纳塔5毫克或10毫克 | 索纳塔20毫克 |
| 首选项 | (n = 344) | (n = 569) | (n = 297) |
| 身体整体 | |||
| 腹部疼痛 | 3. | 6 | 6 |
| 衰弱 | 5 | 5 | 7 |
| 头疼 | 35 | 30. | 42 |
| 不适 | < 1 | < 1 | 2 |
| 光敏性反应 | < 1 | < 1 | 1 |
| 消化系统 | |||
| 厌食症 | < 1 | < 1 | 2 |
| 结肠炎 | 0 | 0 | 1 |
| 恶心想吐 | 7 | 6 | 8 |
| 代谢与营养 | |||
| 外周水肿 | < 1 | < 1 | 1 |
| 神经系统 | |||
| 失忆 | 1 | 2 | 4 |
| 混乱 | < 1 | < 1 | 1 |
| 人格解体 | < 1 | < 1 | 2 |
| 头晕 | 7 | 7 | 9 |
| 幻觉 | < 1 | < 1 | 1 |
| 高渗性 | < 1 | 1 | 1 |
| 感觉减退 | < 1 | < 1 | 2 |
| 感觉异常 | 1 | 3. | 3. |
| 嗜眠症 | 4 | 5 | 6 |
| 地震 | 1 | 2 | 2 |
| 眩晕 | < 1 | < 1 | 1 |
| 呼吸系统 | |||
| 鼻出血 | < 1 | < 1 | 1 |
| 特殊的感觉 | |||
| 视觉异常 | < 1 | < 1 | 2 |
| 耳朵疼痛 | 0 | < 1 | 1 |
| 眼睛疼痛 | 2 | 4 | 3. |
| 听觉过敏 | < 1 | 1 | 2 |
| 嗅觉倒错 | < 1 | < 1 | 2 |
| 泌尿生殖系统 | |||
| 痛经 | 2 | 3. | 4 |
1: Sonata 20 mg治疗患者的发生率至少为1%,且高于安慰剂治疗患者的发生率。大于1%的发生率已四舍五入到最接近的整数。
索纳塔上市前评估期间观察到的其他不良事件
下面列出的是COSTART术语,反映了治疗紧急不良事件的定义不良反应部分。在美国、加拿大和欧洲的上市前2期和3期临床试验中,使用Sonata (zaleplon)治疗的患者报告了这些事件,剂量范围为5mg /天至20mg /天,包括大约2900名患者。所有报告的事件都包括在内,除了那些已经在表1或其他标签中列出的事件,那些药物原因较远的事件,以及那些事件术语过于笼统而没有信息的事件。需要强调的是,尽管报告的事件发生在索纳塔治疗期间,但并不一定是由索纳塔引起的。
事件进一步按身体系统分类,并根据以下定义按频次递减顺序列出:频繁不良事件是指至少1/100例患者中发生一次或多次的不良事件;罕见不良事件是指发生在少于1/100例但至少1/ 1000例患者的不良事件;罕见事件是指发生率低于千分之一的患者。
身体整体-频繁:背痛、胸痛、发热;不常见:胸骨后胸痛,畏寒,面部水肿,全身水肿,宿醉效应,颈部僵硬。
心血管系统——频繁:偏头痛;不常见:心绞痛、束支阻滞、高血压、低血压、心慌、晕厥、心动过速、血管舒张、室性早搏;罕见:双肺、脑缺血、紫绀、心包积液、体位性低血压、肺栓子、窦性心动过缓、血栓性静脉炎、室性心动过速。
消化系统-经常:便秘,口干,消化不良;不常见:发臭、食管炎、胀气、胃炎、肠胃炎、牙龈炎、舌炎、食欲增加、黑化、口腔溃疡、直肠出血、口腔炎;罕见:口腔炎、胆道疼痛、磨牙症、心脏痉挛、口唇炎、胆石症、十二指肠溃疡、吞咽困难、肠炎、牙龈出血、唾液增多、肠梗阻、肝功能检查异常、消化性溃疡、舌头变色、舌头水肿、溃疡性口炎。
内分泌系统-罕见:糖尿病,甲状腺肿,甲状腺功能减退。
血液和淋巴系统-罕见:贫血、淤斑、淋巴结病;罕见:嗜酸性粒细胞增多,白细胞增多,淋巴细胞增多,紫癜。
代谢和营养-罕见:水肿,痛风,高胆固醇血症,口渴,体重增加;罕见:胆红素血症、高血糖、高尿酸血症、低血糖、低血糖反应、酮症、乳糖不耐受、AST (SGOT)升高、ALT (SGPT)升高、体重减轻。
肌肉骨骼系统-常见病:关节痛、关节炎、肌痛;少见:关节病、滑囊炎、关节紊乱(主要是肿胀、僵硬、疼痛)、肌无力、腱鞘炎;罕见:肌炎、骨质疏松。
神经系统-频繁:焦虑、抑郁、紧张、思维异常(主要是注意力难以集中);少见:步态异常、躁动、冷漠、共济失调、口周感觉异常、情绪不稳、欣快、感觉亢进、运动亢进、张力减退、不协调、失眠、性欲减退、神经痛、眼震;罕见:中枢神经刺激、妄想、构音障碍、肌张力障碍、面瘫、敌意、运动障碍、肌阵挛、神经病、精神运动迟缓、下垂、反射减少、反射增加、梦呓、梦呓、口齿不清、昏迷、口齿不清。
呼吸系统-经常:支气管炎;少见:哮喘、呼吸困难、喉炎、肺炎、打鼾、声音改变;罕见:呼吸暂停、打嗝、换气过度、胸腔积液、痰液增多。
皮肤及附属物-频繁:瘙痒、皮疹;少见:痤疮、脱发、接触性皮炎、皮肤干燥、湿疹、斑疹、皮肤肥大、多汗、荨麻疹、水泡性皮疹;罕见:黑变病、牛皮癣、脓疱疹、皮肤变色。
特殊感官-多发病:结膜炎、味觉变态;少见:复视、眼干、畏光、耳鸣、流泪;罕见:调节异常、睑缘炎、白内障、角膜糜烂、耳聋、眼出血、青光眼、迷路炎、视网膜脱离、味觉丧失、视野缺损。
泌尿生殖系统-不常见:膀胱痛、乳房痛、膀胱炎、尿流减少、排尿困难、血尿、阳痿、肾结石、肾痛、月经过多、漏血、尿频、尿失禁、尿急、阴道炎;罕见:蛋白尿、月经延迟、白带、更年期、尿道炎、尿潴留、阴道出血。
上市后报告
过敏/类过敏反应,包括严重反应。
药物滥用和依赖
受管制物质类别
索纳塔被联邦法规列为附表IV管制物质。
虐待、依赖和宽容
虐待和上瘾与身体依赖和耐受性是不同的。滥用的特点是滥用药物用于非医疗目的,通常与其他精神活性物质合用。身体依赖是一种适应状态,表现为一种特定的停药综合征,可由突然停药、剂量迅速减少、药物血液水平下降和/或给药拮抗剂引起。耐受性是一种适应状态,在这种状态下,暴露于药物引起的变化导致一种或多种药物的作用随着时间的推移而减弱。对药物的预期效果和非预期效果都可能产生耐受性,并可能根据不同的效果以不同的速度发展。
成瘾是一种主要的、慢性的神经生物学疾病,遗传、心理社会和环境因素会影响其发展和表现。其特征是行为包括以下一种或多种:对药物使用的控制受损,强迫性使用,不顾伤害继续使用,以及渴望。吸毒成瘾是一种可以利用多学科方法治疗的疾病,但复发很常见。
滥用
两项研究评估了剂量为25mg、50mg和75mg的索纳塔在已知有镇静药物滥用史的受试者中的滥用风险。这些研究的结果表明,索纳塔有滥用潜力类似于苯二氮卓类和苯二氮卓类催眠药。
依赖
在14、28和35个晚上的对照研究和6个月和12个月的开放标签研究中,通过检查停药后反弹性失眠的出现,评估了对索纳塔产生身体依赖和随后戒断综合征的可能性。一些患者(主要是服用20mg的患者)在停药后的第一晚出现轻度反弹性失眠,但似乎在第二晚就消失了。在上市前研究中,使用苯二氮卓类药物戒断症状问卷和检查任何其他戒断-紧急事件,没有发现任何其他证据表明突然停止Sonata治疗后出现戒断综合征。
然而,现有数据无法提供在索纳塔推荐剂量治疗期间依赖发生率的可靠估计。其他镇静/催眠药物与突然停药后的各种体征和症状有关,从轻度不安和失眠到可能包括腹部和肌肉痉挛、呕吐、出汗、颤抖和抽搐的停药综合征。在索纳塔的临床试验中,观察到两名患者癫痫发作,其中一人之前有癫痫发作。动物停用扎来普隆的剂量比建议的人类使用剂量高出许多倍,随后出现癫痫发作和死亡。因为有吸毒或酗酒史的人有习惯和依赖的风险,他们在接受索纳塔或任何其他催眠药时应该受到仔细的监视。
宽容
对索纳塔10mg和20mg催眠效果的可能耐受性进行了评估,方法是在两项28晚安慰剂对照研究中评估索纳塔与安慰剂的入睡时间,以及在一项35晚安慰剂对照研究中评估耐受性在29晚和30晚。在睡眠开始的4周内,未观察到对Sonata的耐受性。
过剂量
关于索纳塔过量的影响,上市前的临床经验有限。报告了两例过量用药。一个是一个2岁半的男孩意外摄入了20毫克到40毫克的扎来普隆。第二例是一名20岁的男性,服用100毫克扎来普隆和2.25毫克三唑仑。两人都接受了治疗,并顺利康复。
迹象和症状
中枢神经系统抑制剂过量作用的体征和症状可预期表现为临床前试验中注意到的药理作用的夸大。过量通常表现为不同程度的中枢神经系统抑制,从嗜睡到昏迷。轻症患者的症状包括嗜睡、精神错乱和嗜睡;在更严重的情况下,症状可能包括共济失调、低张力、低血压、呼吸抑制,很少昏迷,很少死亡。
推荐的治疗
一般的对症和支持措施应配合适当的立即洗胃。需要时应给予静脉输液。动物实验表明氟马西尼是扎来普隆的拮抗剂。然而,在上市前没有使用氟马西尼作为索纳塔过量的解毒剂的临床经验。与所有药物过量病例一样,应监测呼吸、脉搏、血压和其他适当体征,并采取一般性支持措施。低血压和中枢神经系统抑郁应监测和适当的医疗干预治疗。
中毒控制中心
与所有过量用药的管理一样,应考虑多种药物摄入的可能性。医生可能希望与中毒控制中心联系,以获得催眠药物过量管理的最新信息。
用量和给药
索纳塔的剂量应因人而异。对于大多数非老年人来说,索纳塔的推荐剂量是10毫克。对于某些体重较低的人,5毫克可能是足够的剂量。虽然与使用Sonata相关的某些不良事件的风险似乎与剂量有关,但20 mg剂量已被证明是足够耐受的,可以考虑用于偶尔不受益于低剂量试验的患者。超过20毫克的剂量没有得到充分评估,不推荐使用。
应立即在就寝前或在患者已上床睡觉且难以入睡后服用索纳塔预防措施)。在吃一顿高脂肪的大餐时或之后服用索纳塔会导致吸收变慢,并有望减少索纳塔对睡眠潜伏期的影响(见下文的药代动力学)临床药理学).
特殊人群
老年患者和身体虚弱的患者似乎对催眠药的效果更敏感,对5毫克的索纳塔有反应。因此,这些患者的推荐剂量为5毫克。不建议剂量超过10毫克。
肝功能不全:轻度至中度肝功能损害患者应使用索纳塔5mg治疗,因为在该人群中清除率降低。严重肝功能损害患者不建议使用索纳塔。
肾功能不全:轻中度肾功能损害患者无需调整剂量。Sonata在严重肾损害患者中的研究还不够充分。
对于同时服用西咪替丁的患者,应给予5mg的初始剂量,因为在这一人群中,扎来普隆的清除率降低(见下文的药物相互作用)预防措施).
如何提供
索纳塔(zaleplon)胶囊供应如下:
5毫克:不透明的绿色瓶盖和不透明的淡绿色瓶身,瓶盖上写着“5毫克”,瓶身上写着“索纳塔”。
100瓶
10毫克:不透明的绿色瓶盖和不透明的淡绿色瓶身,瓶盖上写着“10毫克”,瓶身上写着“索纳塔”。
100瓶
100个单位剂量包装(10个水泡,每个10粒胶囊)
奏鸣曲®是琼斯制药公司的注册商标。™该公司是King Pharmaceuticals的全资子公司®公司。
储存条件雷竞技到底好不好用
储存在受控的室温下,20°C至25°C(68°F至77°F)。
在USP中定义的耐光容器中分配。
最后更新:2007年11月
索纳塔患者信息表(说白了)
详细资料睡眠障碍的征兆、症状、原因和治疗
本专著中的信息不打算涵盖所有可能的用途、方向、预防措施、药物相互作用或不良反应。此信息是概括性的,不打算作为具体的医疗建议。如果您对正在服用的药物有疑问或想了解更多信息,请咨询您的医生、药剂师或护士。
回:
~所有关于睡眠障碍的文章
APA的参考
Staff, H.(2019年7月30日)。奏鸣曲:治疗失眠(完整的处方信息),HealthyPlace。2021年5月20日,从//www.lharmeroult.com/other-info/sleep-disorders/sonata-to-treat-insomnia-full-prescribing-information获取



